大咖講堂 - 相干拉曼散射顯微術 Ⅱ

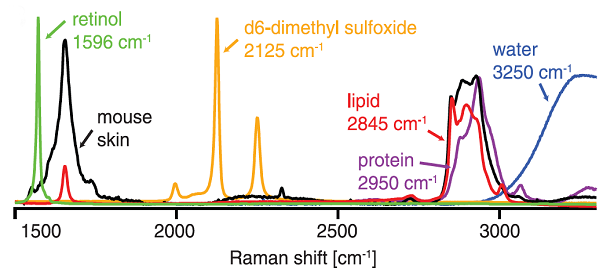
▲圖 1. 常見生物組分和分子的拉曼光譜
快速病理檢測:
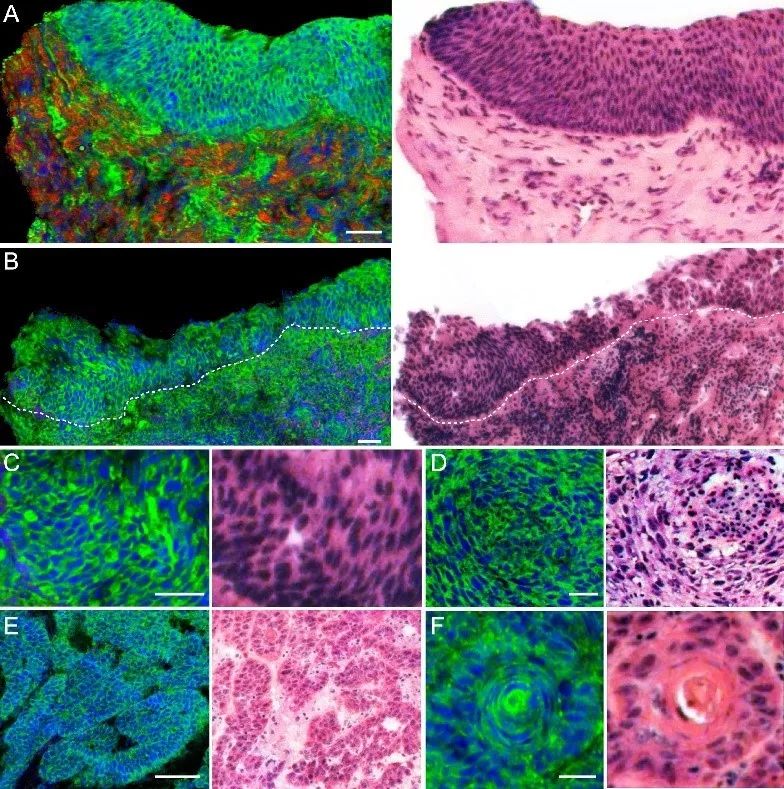
▲圖 2. SRS 與 HE 圖像的一致性對比(綠:脂質;藍:蛋白質;紅:膠原纖維)[3]
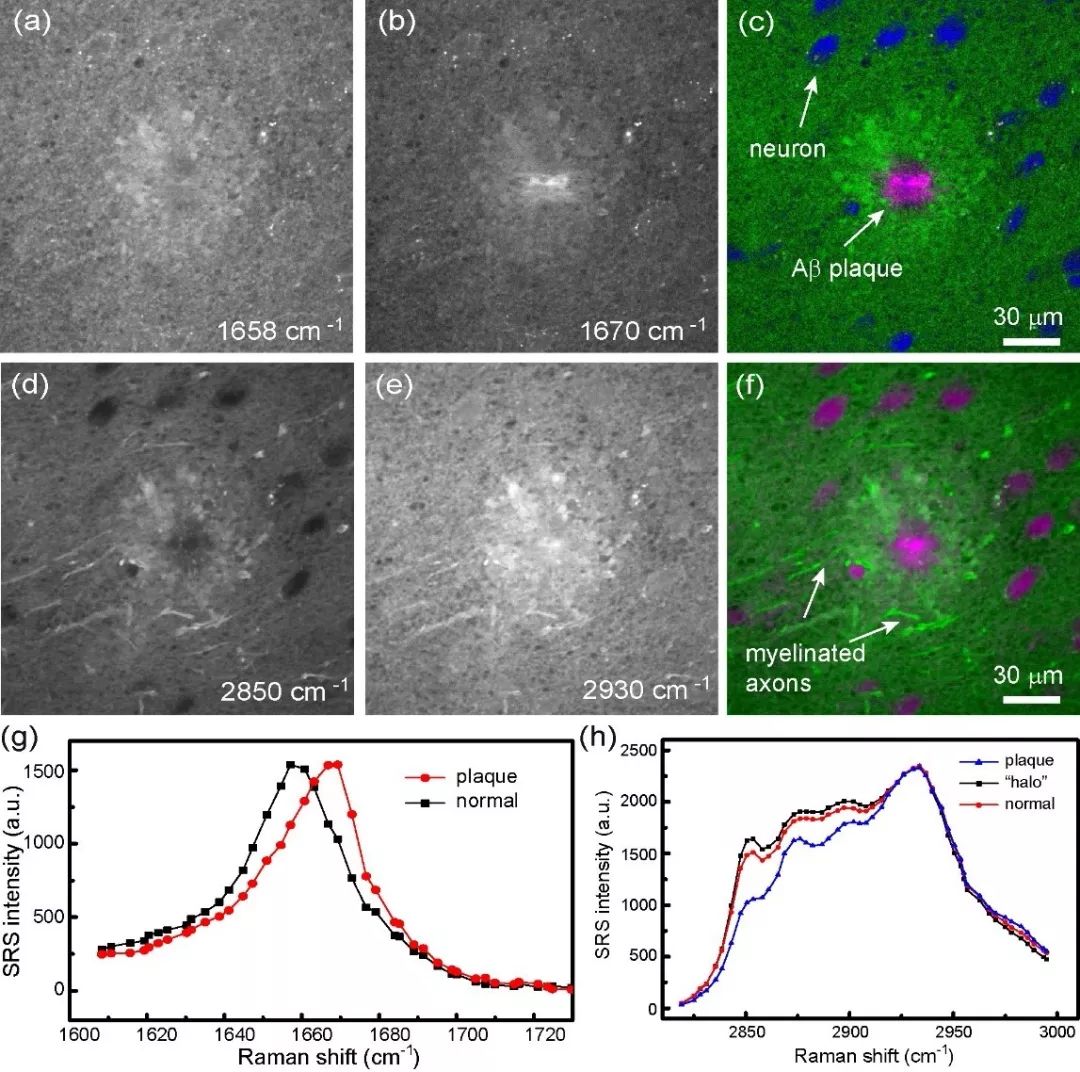
▲圖 3. 新鮮 AD 鼠腦的 SRS 光譜圖像以及斑塊、正常組織的光譜差異 [4]。(a-c)指紋區的光譜圖像,綠:脂質;藍:正常蛋白質;洋紅:淀粉樣蛋白斑塊。(d-f)C-H 伸縮振動區的光譜圖像,綠:脂質;洋紅:總蛋白質。(g-h)不同組織區域的 SRS 光譜
生物代謝:
2018 年,哥倫比亞大學閔瑋教授課題組發展了將重水(D2O)代謝與受激拉曼散射(DO-SRS)顯微技術相結合的技術,用于原位代謝觀測[5] 。在生物代謝過程中,經過酶的催化合成,D2O 中的氘原子會被自動整合到有機分子中,形成同位素標記的 C-D 鍵。因此,基于對新合成有機分子中 C-D 鍵的成像,就可以實現生物代謝的追蹤觀測(視頻 1)。目前,在 C-D 鍵的廣泛振動光譜中,他們發現了脂質和蛋白質的特異性拉曼位移,并開發了光譜解調方法來獲得具有大分子選擇性的 C-D 信號,做到了在動物模型中脂質、蛋白甚至糖類的代謝測量[6][7]。
▲視頻 1.秀麗隱桿線蟲的脂質 SRS 實時成像(左:原本存在的脂質;右:利用 D2O 新合成氘代脂質)[5]
藥物運輸:
在醫藥學中,藥物的運輸是學者們關注的重點之一,準確地運輸過程及定位,是藥物分子能實現特定生理功能的重要保障。制作小分子藥物的熒光標簽并非容易之事,常用的熒光標簽往往比藥物分子大很多,這會影響他們的運輸特性;因此,利用傳統熒光標記方法追蹤小分子藥物面臨很多挑戰。而很多藥物分子本身具有特殊的化學鍵振動(圖 4),因此,利用 SRS 可以對該藥物進行很好的特異性成像,加之 SRS 不需要對樣品固定、染色等操作,最大程度上保持了生物體樣品的活性,可以實現系列活體動態捕捉。
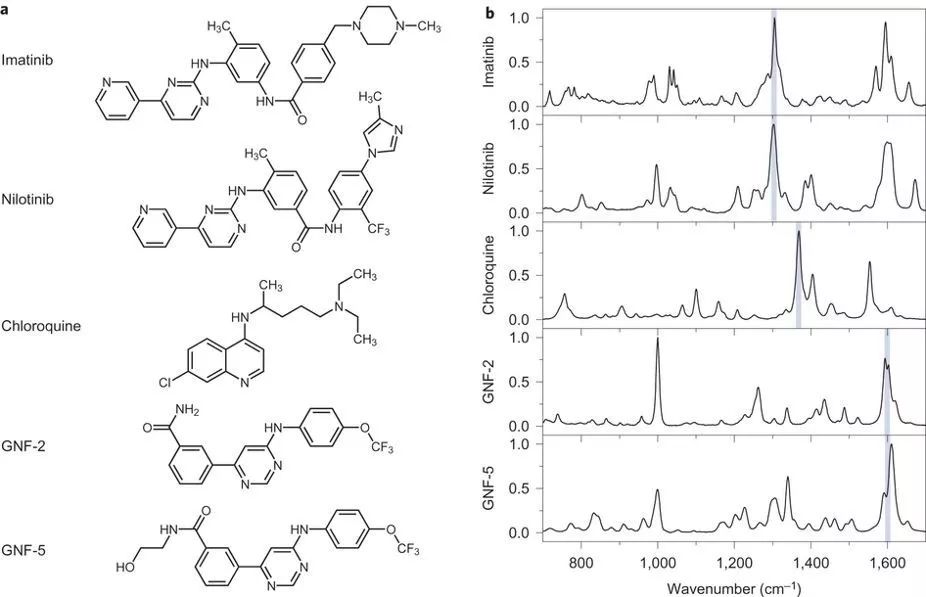
▲圖 4. 藥物分子的結構式及其拉曼光譜 [9]
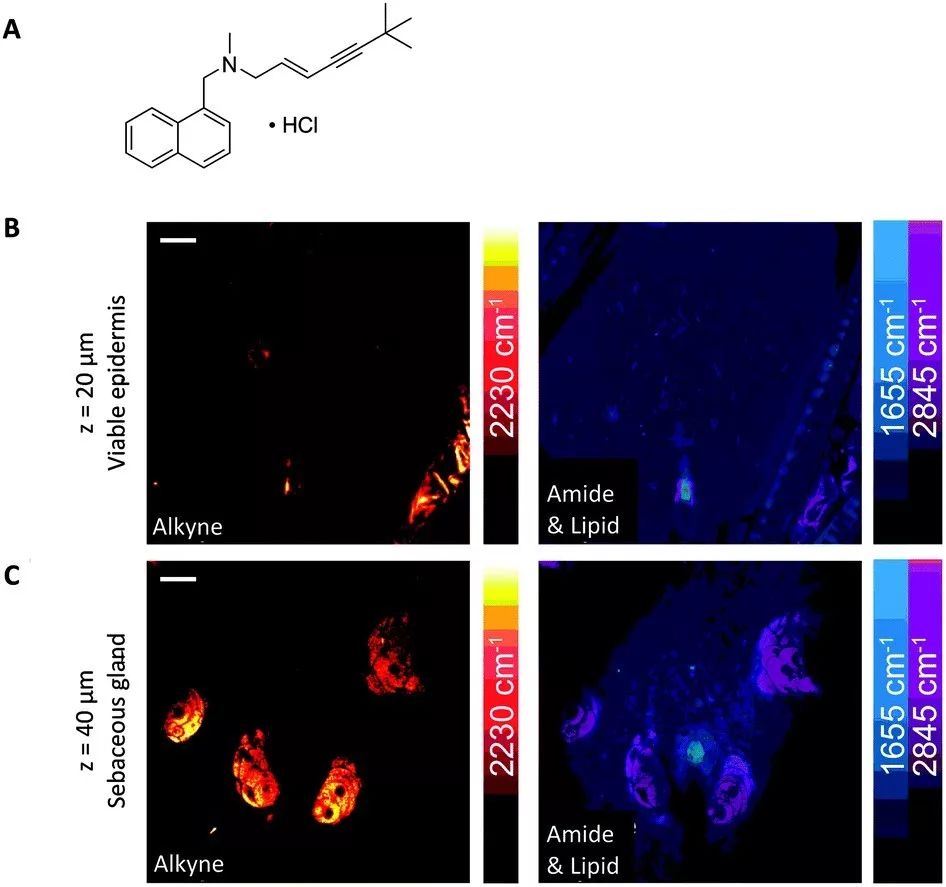
▲圖 5.局部應用鹽酸特比萘芬對小鼠耳部皮膚的 SRS 成像(2230cm-1:鹽酸特比萘芬;1655cm-1:蛋白質;脂質 2845cm-1:脂質)[8]
參考文獻:
(上下滑動查看所有參考文獻)
作者簡介
季敏標,男,1982 年出生于浙江省臺州市。2001 年獲北京大學物理系學士;2011 年獲美國斯坦福大學物理系博士學位,研究方向為非線性光學和超快分子動力學;之后在哈佛大學謝曉亮組里從事博士后研究(2011-2014),發展相干拉曼成像技術并將其應用到腫瘤的無標記探測。2014 年入職復旦大學物理系擔任研究員和博士生導師。2015 年入選中組部“千人計劃”(青年組)和上海市“青年科技啟明星計劃”。
季教授的研究方向集中在非線性光譜學在物理、化學和生物醫學等交叉學科中的應用,研究課題包括利用新型光譜顯微成像技術研究生物醫學問題,以及新材料的光電子特性研究等。迄今發表 SCI 論文 50 余篇,包括 Science, Science Translational Medicine, Science Advances, PNAS 等。并承擔科技部重點研發計劃“數字診療裝備”青年專項、基金委面上項目、上海市科技創新行動計劃等多項科研項目。
作為一款成熟的商品化 CRS 產品,徠卡 TCS SP8 CARS 共聚焦顯微鏡可以簡單快速地實現 CARS 無標記成像、單光子/多光子共聚焦熒光成像、二次(SHG)/三次(THG)諧波成像,或者使用紅外、紫外激光進行的各種應用的成像,滿足全方位、多維度的高級生命科學研究需要。




